Sommaire
L’adoucisseur échangeur d’ions
Au départ, la présence de calcaire
L’eau est un solvant très efficace ! au contact de l’atmosphère elle capte du CO2 et devient légèrement acide (H2CO3). Par percolation au travers des sols, elle entre en contact avec la roche calcaire CaCO3, qu’elle dissous.
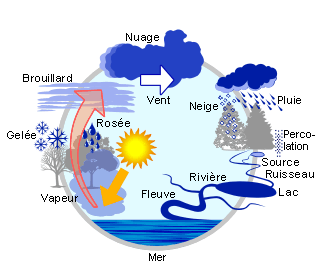
Le carbonate de calcium CaCO3 présent dans l’eau va précipiter sur les parois lors d’une montée en température de celle-ci.

L’adoucisseur est dès lors un appareil destiné à capter les ions Ca++ et Mg++ présents dans l’eau en les fixant sur une résine cationique. En effet, l’eau passe au travers d’une cartouche contenant des millions de petites billes de résine, chargées d’ions sodium.
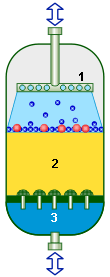
Adoucisseur.
- Distributeur d’eau et de solution de régénération
- Résine échangeuse d’ions
- Plancher à buses (crépines) avec fentes de 0,4 mm
Par exemple, il peut s’agir de la zéolithe, silicate d’Al et de Na :
Na2O . Al2O3. n SiO2. m H2O
On dira en abrégé : Na2Z
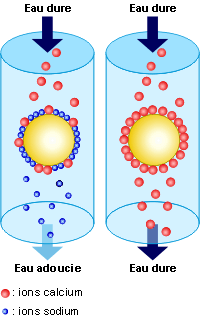
Au passage de l’eau sur cette résine, les ions calcium seront captés :
Na2Z + Ca++ –> CaZ + 2 Na+
ou encore :
Na2Z + Ca(HCO3)2 –> CaZ + 2 Na(HCO3)
De même pour les ions magnésium :
Na2Z + Mg(HCO3)2 –> MgZ + 2 Na(HCO3)
Remarque : le sel sodique produit (Na (HCO3)) passera dans l’eau mais ne contribuera pas à la dureté de l’eau; si la température augmente, il ne se dépose pas.
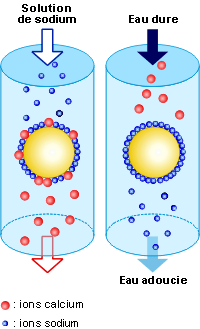
Régénération
Lorsque la résine est saturée en ion Ca++, il faut les éliminer et replacer les ions Na+. C’est la phase de régénération :
CaZ + 2 NaCl –> Na2Z + CaCl2
Prolifération de micro-organismes
Les échangeurs d’ions offrent, comme d’autres filtres, de bonnes conditions de prolifération aux micro-organismes en raison de l’importante surface de leurs pores internes. Si aucune mesure n’est appliquée, on constate donc souvent une augmentation de la teneur en bactéries de l’eau traitée. La prolifération microbienne peut être combattue de façon efficace par l’adjonction d’environ 1 % de résine échangeuse d’ions imprégnée d’argent.
La corrosion des eaux trop adoucies
L’eau adoucie présente une concentration en calcium proche de zéro. Dès lors, l’équilibre calco-carbonique rend l’eau très agressive (les dépôts calcaires protecteurs sont rapidement dissous). On conseille dès lors de ne pas adoucir l’eau en dessous des 15°F, soit grâce à un réglage de l’adoucisseur, soit par le placement d’un bypass qui réalise un mélange entre de l’eau traitée et de l’eau totalement adoucie.
Attention à la propreté des sels
Si des impuretés sont mélangées au sel de régénération (bacs restant ouverts…), elles pourront servir de nutriments aux bactéries et tout paraticulièrement à la légionelle !
Les inhibiteurs de tartre
Le principe consiste à inhiber l’entartrage plutôt qu’à éliminer le calcium, par l’injection d’un produit chimique, tel que le polyphosphate qui va se dissoudre dans l’eau et enrober chaque ion calcium d’un “manteau” d’ion phosphate. La croissance des cristaux calcaires est freinée et/ou leur adhésion est empêchée sur les parois.
Mais ce produit est avalé avec l’eau par le consommateur… le contrôle de la concentration doit être rigoureux !
De plus, les polyphosphates n’agissent plus si l’eau est trop chaude.
Le CSTB en France a réalisé récemment une étude sur ce sujet.
Les systèmes physique et/ou magnétique
L’appareil agit par effet électrique et/ou magnétique et transforme le calcium en aragonite (une variété cristalline du carbonate de calcium), plus stable et donc donnant moins lieu à des dépôts.
Certains de ces systèmes ont des effets réels mais variables en fonction de divers paramètres (température, débit, intensité électrique,….) si bien qu’il est difficile de prévoir avec certitude le résultat de leur action dans des conditions particulières.
Pour plus d’informations sur ces différentes techniques, on consultera utilement le Cours – conférence n°51 du CSTC – “la corrosion et les tubes métalliques utilisés pour la distribution d’eau dans les bâtiments”.
![Adoucisseur d'eau [Stérilisation] Adoucisseur d'eau [Stérilisation]](https://energieplus-lesite.be/wp-content/uploads/2007/09/sterilisation-02-800x420.jpg)





Auteur : les anciens
Mars 2009 : Thibaud
Notes :
16/03/09, par Julien :
Avril 2009, Sylvie :
Mai 2009